전립선암을 치료하기 위한 일반적인 접근 방법은 항안드로겐제의 투여입니다. 안드로겐 수용체에 안드로겐 대신 결합하여 안드로겐의 작용을 억제하는 원리로 이러한 원리는 길항제(antagonist)라고 불립니다.
항안드로겐제 종류
1세대 항안드로겐제
잘 알려진 약물로는 1세대 항안드로겐제로 알려진 비칼루타미드(bicalutamide), 플루타미드(flutamide), 닐루타미드(nilutamide)가 있습니다.
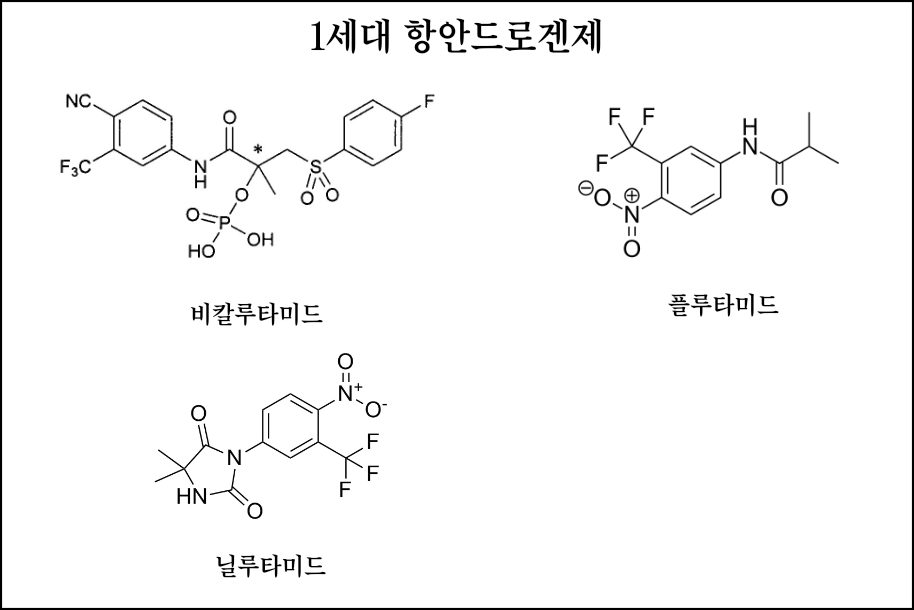
AR 억제에 대한 1세대 항안드로겐제는 AR 리간드 활성화를 차단하기 위한 스테로이드 유사체입니다. 그러나 이러한 억제제에 대한 내성이 생겼다는 사실이 금방 드러났습니다. 1차 약물 내성 메커니즘은 AR 증폭, 점 돌연변이, 리간드 독립적인 AR 스플라이스 변이체의 발현, 종양 내 안드로겐 생산 또는 다운스트림 신호 전달 메커니즘에서 발생하는 것으로 믿어집니다.
2세대 항안드로겐제
2세대 안드로겐 억제제로는 아비라테론(abiraterone), 엔잘루타마이드(Enzalutamide), 다롤루타마이드(Darolutamide)), 아팔루타마이드(Apalutamide)가 있습니다.
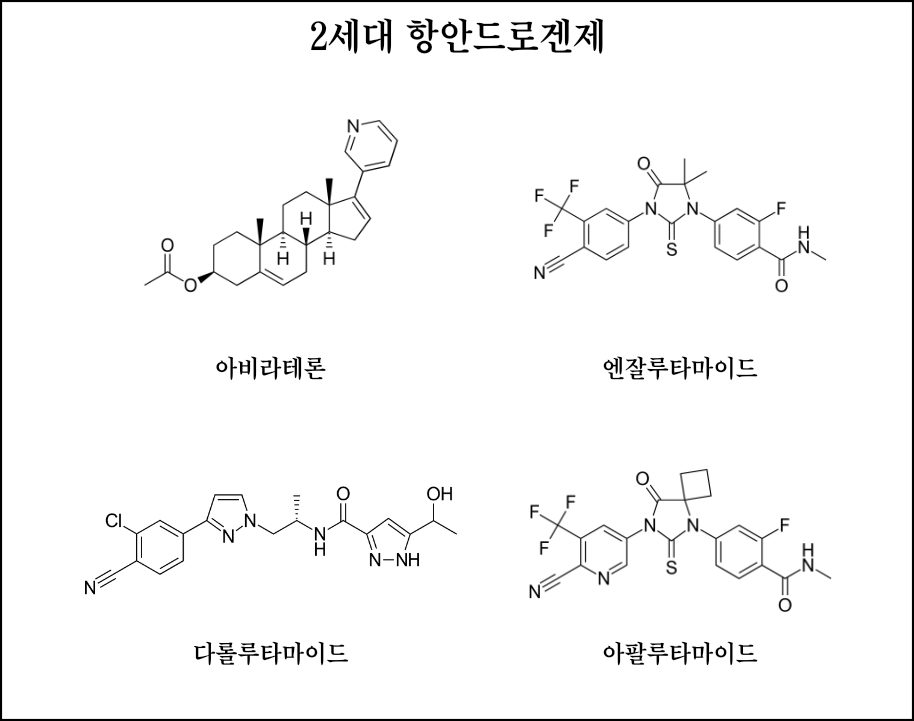
아비라테론(abiraterone)은 최초의 경구용 전이성 거세저항성 전립선암 치료제로, 고환과 부신, 전립선암세포 등 남성 호르몬인 안드로겐이 생성되는 모든 경로를 차단해 암 진행을 지연시킨다.
2세대 항안드로겐제가 개발되기 전까지, CRPC에 대한 가장 효과적인 치료 전략은 탁산 화학요법제인 도세탁셀(docetaxel)과 카바지탁셀(cabazitaxel)이었습니다.
또 다른 치료법으로는 시풀류셀-T(프로벤지) 백신을 이용한 면역요법이 있습니다.
2세대 antiandrogens에는 다른 steroidal 수용체에 안드로겐 수용체에 증가한 특이성이 있고, 이전 세대 보다는 더 높은 친화력에 행동하고, AR에 독점적으로 길항작용이고, 차례로 안드로겐 철수 증후군을 이끌어 내지 않습니다. 이러한 화합물은 환자 수명을 크게 늘리고, 전이가 없는 전체 생존을 연장하고, 순환 및 종양 내 안드로겐 및 혈청 PSA를 감소시켰습니다. 이러한 발전에도 불구하고 CRPC는 근절되지 않았습니다.
2세대 항안드로겐은 다른 스테로이드 수용체에 비해 안드로겐 수용체에 대한 특이성이 증가하고, 이전 세대보다 더 높은 친화력으로 작용하며, 독점적으로 AR에 길항하고, 차례로 안드로겐 금단 증후군을 유발하지 않습니다. 2세대는 독성을 줄이고, 환자의 수명을 증가시켰고, 종양 내 안드로겐 및 혈청 PSA를 감소시켰지만, CRPC를 완전히 정복하진 못했습니다.
내성과 병용 투여
호르몬 반응성 고위험 전이성 전립선암(mHSPC)으로 새롭게 진단된 환자의 치료에 안드로겐 차단요법(ADT)과 병용 투여한다.
항암제에 대한 내성은 항안드로겐제에만 적용되는 문제는 아닙니다. 다른 암뿐만 아니라 바이러스 감염에 이르기까지 다양한 질병에서 이루어지고 있습니다.
